【業績會直擊】先聲藥業(2096.HK):創新藥收入大增,估值邏輯或已改變
2021年8月26日,先聲藥業(2096.HK)發佈半年業績報吿,並於近日召開業績溝通會議。董事長任晉生、CFO萬玉山、常務副總裁唐任宏、董祕鮑軍出席該會議。
2021中期公司業績溝通會
在先聲藥業的中期業績中,其與“創新”相關的幾組數據均表現亮眼。2021年上半年公司收入約21.2億元人民幣,同比增長10.1%。其中創新藥(先必新+恩度+艾得辛+恩瑞舒)收入約為12.2億元,佔同期收入比例高達57.6%,創新藥收入金額較去年同比增長達56.8%。這些數據一改先聲以往仿製藥為主的老牌藥企形象,創新成色愈發鮮明。
除此之外,先聲對於創新研發的投入也可謂大手筆,2021年上半年研發投入約6.27億元,較去年同比增長38%,佔收入比例高達29.6%。這也從另一個角度説明了先聲快速向創新轉型的決心與速度。
圖表一:2018-2021H1公司創新藥收入佔比
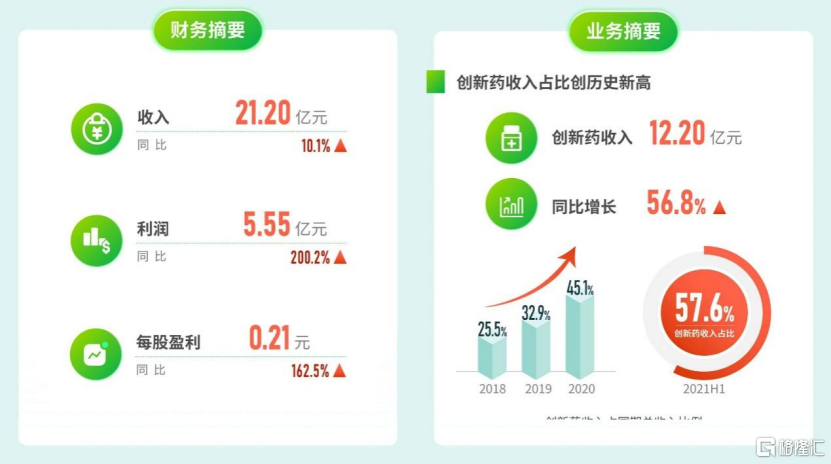
數據來源:公司資料,格隆彙整理
創新藥研發進展飛速,11種創新藥處於臨牀階段
先聲藥業重點聚焦於“中樞神經、自身免疫、腫瘤”三大疾病領域,擁有多元化的創新產品組合,已有超過40款產品被納入醫保。本次中期業績發佈距先聲於2020年10月港交所上市尚不足1年,但通過前後對比可以看出,其創新產品管線已發生諸多變化,研發進展迅速。截至2021年6月30日,公司共擁有項目近60項,其中11種創新藥產品處於臨牀研究階段。
圖表二:先聲藥業上市至現在創新藥品研發進展對比圖
先聲藥業上市時產品管線圖:
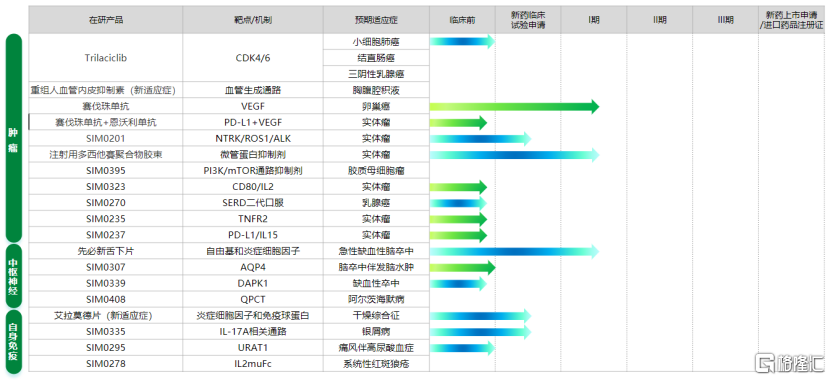
先聲藥業中期業績發佈時產品管線圖:
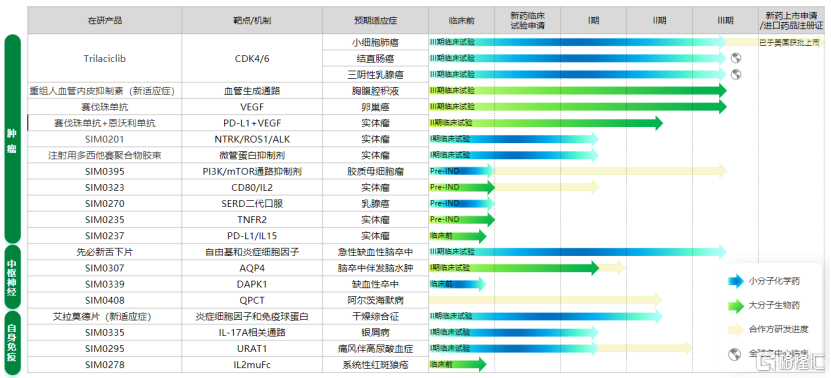
數據來源:公司資料,格隆彙整理
成熟的商業化推廣能力,醫保落地後先必新快速放量
從不同疾病領域來看,上半年,公司來自中樞神經系統疾病藥物組合(主要產品為先必新®等)的收入達人民幣5.95億元,佔本集團總收入約28.1%。腫瘤疾病藥物組合(主要產品為恩度®等)的收入達約5.53億元,佔公司總收入26.1%。自身免疫疾病藥物組合的收入達約3.17億元,佔公司總收入約15%。其他領域產品收入達約4.8億元,佔公司總收入約22.6%。
在中樞神經領域藥物中,於2020年7月上市的先必新®(依達拉奉右莰醇注射用濃溶液)是全球近5年以來唯一獲批銷售的腦卒中新藥,並已納入國家醫保,該醫保目錄於今年3月正式執行後,先必新銷量迅速攀升,上市一週內已實現入院超1700家。此外,先必新還有一個舌下片劑型也在III期臨牀試驗中,舌下含服的給藥方式不受醫療場所條件和依從性限制,對患者更加便捷,未來也更適於拓展其他慢性中樞神經系統疾病適應症。
在自身免疫系統藥物中,艾得辛是全球首個上市、國內唯一上市的艾拉莫德藥物,適應症為類風濕性關節炎。目前正在拓展新的適應症:乾燥綜合徵,並已進入II期臨牀實驗。阿巴西普是中國首個及唯一獲批准銷售的CTLA4-Fc融合蛋白,並且也是現在唯一的T細胞選擇性共刺激免疫調節劑,對於抗環瓜氨酸肽抗體(ACPA)陽性患者更優效。
在腫瘤領域藥物中,恩度®為一種重組人血管內皮抑制素注射液,不僅是中國第一個抗血管生產靶向藥,也是國內首個獲批的非小細胞肺癌一線治療生物創新藥。除此之外,其還是國內外唯一獲准銷售的內皮抑制素,已進入國家醫保目錄多年。公司正在積極拓展恩度®用於治療惡性胸腹腔積液的新適應症,目前正在全國開展多中心的III期臨牀研究。
自主研發與合作研發雙輪驅動,佈局高未滿足領域
先聲藥業的BD能力一向為業界所稱道,其與美國G1公司的合作也受到了業內廣泛關注。Trilaciclib是一款用於化療前骨髓保護的小分子FIC創新藥。自2020年8月雙方宣佈聯盟後,其後快速取得諸多里程碑。今年1月,CDE批准該藥用於小細胞肺癌的臨牀試驗,4月和6月,該藥又分別獲批2項III期臨牀試驗,分別用於轉移性結直腸癌和三陰性乳腺癌。
2021年上半年,先聲也達成了2項重磅Lisence-in項目:3月,與Kazia公司就膠質母細胞瘤產品Paxalisib達成合作;6月,先聲又與Vivoryon公司就靶向毒性澱粉樣蛋白N3pE的2款產品達成協議,這也是先聲在阿爾茲海默症領域的首次嘗試。
在先聲的研發管線中,還有幾款處於臨牀階段的產品各具特色,值得關注:
(1)賽伐珠單抗,是新一代重組人源化抗血管內皮生長因子(抗VEGF)單克隆抗體,目前正在中國開展卵巢癌III期臨牀試驗。
(2)SIM0295,是一種高選擇性的強效尿酸鹽轉運蛋白1 (URAT1) 抑制劑,可開發用於治療痛風伴高尿酸血癥。目前合作方JW公司已完成IIb期臨牀。先聲擬於中國開展III期臨牀試驗。
(3)SIM0201,是先聲主研發的針對NTRK、ROS1或ALK融合突變的強效多靶點酪氨酸激酶抑制劑,可透過血腦屏障,對腦轉移腫瘤有效。目前正處於I期劑量探索階段。
(4)SIM0335,是先聲主研發的創新小分子藥物,也是全球首款調控脂肪酸代謝作用於IL-17A相關通路的國家I類候選新藥,旨在通過外用方式治療輕度至中度的斑塊狀銀屑病患者。目前正在開展I期臨牀試驗研究。
(5)SIM0307 是基於諾貝爾獎成果水通道學説開發出的一種水通道蛋白4 (AQP4)抑制劑,作為腦水腫領域全新作用機制的小分子First-in-class(首創)新藥,擬用於治療急性重症缺血性腦卒中伴發腦水腫。先聲正於中國開展I期臨牀實驗研究。
Q&A環節
Q1:現在很多傳統藥企也在加大BD力度,公司在BD佈局上有哪些優勢?此外,公司對吸引新項目及新人才有哪些激勵政策?
A1:公司在BD方面持續加強,目前已擁有超25人,在中國、美國、歐洲均有分支機構的成熟團隊。目前公司海外的BD基本以外籍人員為主。在項目研發上,公司有副總裁專門負責外部研發管理。工作流程上,BD團隊與研發、戰略、市場、銷售等多個部分都有密切的交流和聯繫。
在人才激勵方面,公司除了基礎的薪酬和獎金,還有股權激勵及項目激勵。公司希望員工以長期的心態,與先聲共同奮鬥與發展。今年公司已陸續公佈了部分股權激勵計劃,未來還將持續推進。
Q2:關於公司的URAT1抑制劑項目中,該靶點是否存在潛在副反應較大的情況?研發成功率如何估計?新型URAT1與苯溴馬隆抑制劑在分子設計及機制上有何區別?
A2:URAT1抑制劑SIM0295和苯溴馬隆抑制劑是一個同靶點,但在分子設計上有所不同。目前從韓國已開展的IIa/IIb實驗數據以及中國所做的試驗數據來看,該分子毒性可控。公司將於2021年下半年,參照合作伙伴已產生的IIb期臨牀數據,選擇合適的對照組在國內開展III期臨牀。
Q3:公司對於PD-L1上市的預期如何?
A3:恩沃利單抗是一種PD-L1單域抗體Fc融合蛋白,公司與思路迪和康寧傑瑞於去年簽訂三方合作協議,獲得了恩沃利單抗在中國大陸於腫瘤治療所有適應症方面的獨家推廣權。預計恩沃利單抗有望於今年下半年上市,併成為全球首個皮下注射PD-L1。
公司多個部門已與外部機構合作,對於PD-L1市場做了大量前期調研,對該領域進行了深入瞭解。公司認為,恩沃利單抗這款PD-L1皮下給藥的方式獨具特色,不受住院治療的限制,可與口服治療藥物聯用,滿足患者對藥物可及性的需求。雖然對PD-L1的單價預期下降,但因此惠及更多患者、覆蓋範圍更廣也是肯定的。該產品的上市也將會推動公司在腫瘤領域的隊伍進一步擴增,進而與後續腫瘤新產品在商業化方面協同增效。